FDAが IEC 61326-2-6:2025(Ed.4) を認知規格に登録
 EU/米国情報
2025.08.08
EU/米国情報
2025.08.08
2025年7月28日付けで米国FDAの認知規格リストに
IEC 61326-2-6:2025(Ed.4) が掲載されました。
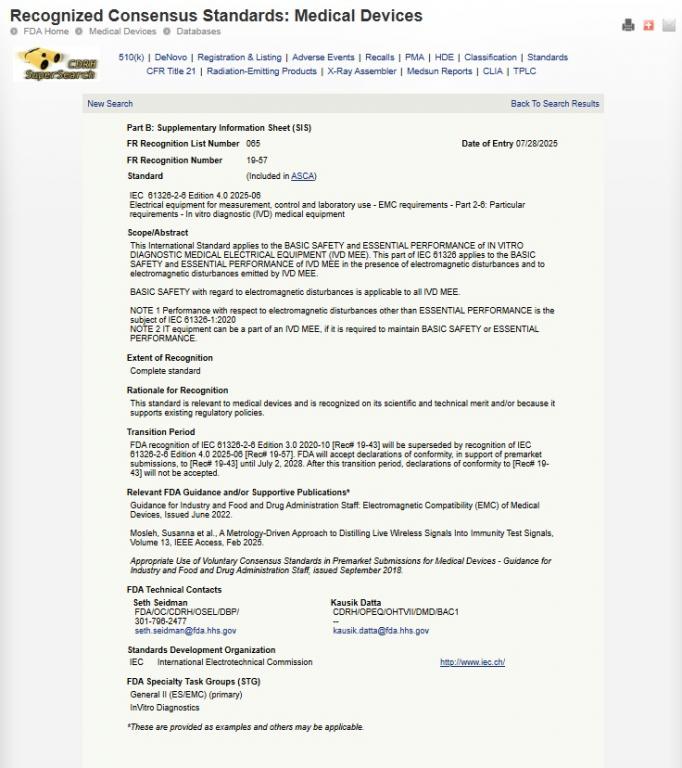
Scope/Abstract
This International Standard applies to the BASIC SAFETY and ESSENTIAL PERFORMANCE of IN VITRO DIAGNOSTIC MEDICAL ELECTRICAL EQUIPMENT (IVD MEE). This part of IEC 61326 applies to the BASIC SAFETY and ESSENTIAL PERFORMANCE of IVD MEE in the presence of electromagnetic disturbances and to electromagnetic disturbances emitted by IVD MEE.
BASIC SAFETY with regard to electromagnetic disturbances is applicable to all IVD MEE.
NOTE 1 Performance with respect to electromagnetic disturbances other than ESSENTIAL PERFORMANCE is the subject of IEC 61326-1:2020
NOTE 2 IT equipment can be a part of an IVD MEE, if it is required to maintain BASIC SAFETY or ESSENTIAL PERFORMANCE.
【参考訳】
範囲/概要
この国際規格は、体外診断用電気医療機器(IVD MEE)の基礎安全および基本性能に適用されます。IEC 61326のこの部分は、電磁妨害が存在する場合のIVD MEEの基礎安全および基本性能、ならびにIVD MEEから放射される電磁妨害に適用されます。
電磁妨害に関する基礎安全は、すべてのIVD MEEに適用されます。
注1:基本性能以外の電磁妨害に関する性能は、IEC 61326-1:2020の対象です。
注2:IT機器は、基礎安全または基本性能の維持が求められる場合、IVD MEEの一部となり得ます。
旧規格の IEC 61326-2-6:2020(Ed.3) は
2028年7月2日まで受け付ける
とされています。



